Presencia de microsporidio hepatopancreático hace al camarón blanco del Pacífico susceptible a AHPND, SHPN

El microsporidio hepatopancreático intracelular Enterocytozoon hepatopenaei (EHP) ha sido reportado en el cultivo de camarón tigre negro (Penaeus monodon) y de camarón blanco del Pacífico (P. vannamei) en China, Indonesia, Malasia, Vietnam, Tailandia y la India, así como en otros países del sudeste asiático.
EHP causa retardo en el crecimiento y mayor variabilidad de tallas, y en estadios más avanzados, los camarones infectados tienen cáscaras blandas y exhiben letargo, alimentación reducida y tractos digestivos-medios vacíos. Actualmente, el EHP se diagnostica por histología, hibridación In-situ y PCR.
Durante el año 2009-2012, una nueva enfermedad emergente llamada Enfermedad de Necrosis Hepatopancreática Aguda (AHPND), también conocida como Síndrome de Mortalidad Temprana (EMS), comenzó a provocar mortalidades significativas en el camarón y pérdidas de producción en la mayoría de los países donde se había reportado EHP. En algunos casos, el AHPND también fue reportado en co-infección con EHP. Se determinó que los agentes causales de AHPND eran bacterias Vibrio incluyendo Vibrio parahaemolyticus, V. campbellii, V. owensii y V. harveyi.
Algunos países asiáticos productores de camarón, especialmente India e Indonesia, sólo han sido afectados por EHP, y hasta el momento no se han notificado casos de AHPND. Estos países han visto un aumento de los problemas bacterianos que contribuyen a la Vibriosis del hepatopancreas, que ha sido ” síndrome de mortalidad en marcha” y “síndrome de heces blancas.” Los camarones afectados por estas condiciones muestran necrosis hepatopancreática séptica (SHPN).
Debido a que el EHP ha estado afectando a la industria del cultivo de camarón antes de la aparición de brotes de AHPND, es posible que el EHP favorezca el establecimiento de AHPND y otras enfermedades bacterianas, como SHPN. Para determinar la relación de EHP con AHPND y SHPN – y apoyados por el Instituto Nacional de Alimentación y Agricultura de los Estados Unidos bajo el proyecto N º ARZT – 5704190 – A50-126 – evaluamos el factor de riesgo de EHP con estas enfermedades: AHPND a través de pruebas experimentales, y SHPN por un análisis de casos y controles. Este artículo resume la publicación original [Aquaculture 471 (2017) 37-42)].
Configuración del estudio
Se utilizaron animales Penaeus vannamei libres de patógenos específicos (SPF) de una instalación comercial (Shrimp Improvement Systems en Islamorada, Fla.). Las infecciones experimentales se llevaron a cabo en el Laboratorio de Patología Acuícola (APL), Universidad de Arizona (EE.UU.). Consulte la publicación original o póngase en contacto con el primer autor para obtener una descripción detallada de los diversos experimentos para propagar la infección por EHP en camarones SPF en el APL; las cepas bacterianas y cultivo de AHPND; los bioensayos de patogenicidad e histopatología de AHPND; los conteos bacterianos e histopatología en un curso de infección de 12 horas; la relación entre la microsporidiosis hepatopancreática (HPM) y la necrosis hepatopancreática séptica (SHPN) a nivel de granja; la histopatología e hibridación In situ (ISH) para EHP; ensayos de PCR para EHP y AHPND; y los análisis estadísticos utilizados en este estudio.
Resultados
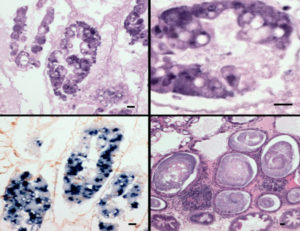
En relación a la infección por EHP antes de la infección por AHPND, EHP se confirmó mediante histopatología en muestras de camarón pre-infectado de EHP y en el grupo de control EHP negativo. La severidad de la infección varió entre G1 y G2 basándose en una escala semi-cuantitativa. La infección fue más prominente en las regiones medial y proximal que en la región distal. Antes de la infección experimental, no se observaron lesiones de AHPND en ningún animal.
La Tabla 1 muestra los resultados de la infección experimental con VPAHPND. No se observó mortalidad en los tanques de control negativo en los dos experimentos. Confirmado por PCR e histopatología, el VPAHPND utilizado en este experimento causó AHPND en los animales infectados. Los grupos expuestos a una dosis alta de V. parahaemolyticus tuvieron una alta mortalidad (83 por ciento y 64 por ciento).
Aranguren, EHP, Tabla 1
| Experimento | Grupo Experimental | Tratamiento | Dosis (CFU/mL agua) | No. camarones muertos/No. total | Mortalidad (%) |
|---|---|---|---|---|---|
| 1 | AHPND | Dosis baja | 2.4 X 10 (5th poder) | 0/5 | 0 |
| 1 | EHP-AHPND | Dosis baja | 2.4 X 10 (5th poder) | 3/5 | 60 |
| 1 | Control positivo | Dosis alta | 2.4 X 10 (6th poder) | 5/6 | 83 |
| 1 | Control de tanque | Control negativo EHP | 0 | 0/5 | 0 |
| 1 | Control de tanque | Control negativo SPF | 0 | 0/5 | 0 |
| 2 | AHPND | Dosis baja | 2.4 X 10 (5th poder) | 2/11 | 18 |
| 2 | EHP-AHPND | Dosis baja | 2.4 X 10 (5th poder) | 4/9 | 44 |
| 2 | Control positivo | Dosis alta | 2.4 X 10 (6th poder) | 7/11 | 64 |
| 2 | Control de tanque | Control negativo EHP | 0 | 0/5 | 0 |
| 2 | Control de tanque | Control negativo SPF | 0 | 0/5 | 0 |
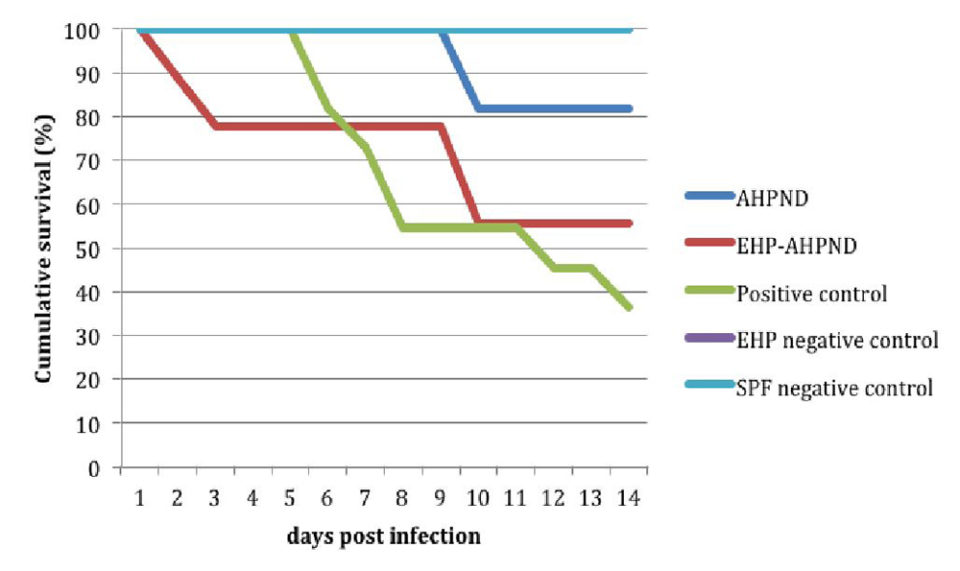
Cuando los juveniles del grupo EHP-AHPND (camarones pre-infectados por EHP infectados con VPAHPND) fueron desafiados con una dosis baja, tuvieron mortalidades más altas – 60 por ciento frente a 0 por ciento y 44 por ciento frente a 18 por ciento en los experimentos No. 1 y No. 2, respectivamente – que los del grupo AHPND (camarones infectados con VPAHPND).
La Fig. 1 muestra una comparación de las curvas de supervivencia entre los grupos AHPND frente a EHP-AHPND y se encontró una diferencia significativa (P <0,05).
Los animales moribundos examinados por histología tenían lesiones típicas de AHPND, incluyendo un desprendimiento masivo de células epiteliales de túbulos hepatopancreáticos en las regiones medial y proximal del hepatopancreas, y progresando hacia afuera a la región distal. La fase terminal (caracterizada por un SHPN típico) fue observada en algunos animales.
Los animales muertos se analizaron por PCR para AHPND y EHP. En el grupo AHPND y los tanques de control positivo, sólo se encontraron resultados positivos de AHPND. En el grupo EHP-AHPND, los camarones fueron positivos tanto para AHPND como para EHP. Los camarones sobrevivientes del experimento no presentaron ninguna lesión histopatológica de AHPND.
En el experimento de histopatología y conteo bacteriano (curso de infección de 12 horas), no se observaron lesiones histológicas de AHPND en el grupo AHPND durante las primeras 6 horas después de la infección (h.p.i.); dos animales mostraron una fase temprana de lesiones de AHPND con un grado de gravedad G1 a las 12 h.p.i.
![A la izquierda: Histología de WFS, Heces Blancas - H&E. Derecha: hibridación In situ para EHP en WFS [Heces Blancas - ISH (EHP)]. De: Tang et al. (2016).](https://www.globalseafood.org/wp-content/uploads/2017/05/ARANGUREN-Pic-2-300x213.jpg)
En comparación con la ISH, no todas las células desprendidas tuvieron una reacción positiva para EHP, lo que sugiere que el desprendimiento estaba presente en células infectadas con EHP y células no infectadas con EHP. A las 12 h.p.i., hubo una ausencia de células B, la necrosis progresó hacia la región distal y ocurrió un desprendimiento masivo. A las 12 h.p.i., el 57 por ciento de los camarones del grupo EHP-AHPND mostraron AHPND frente al 11 por ciento del grupo AHPND. No se encontraron signos histológicos de AHPND en camarones del control negativo.
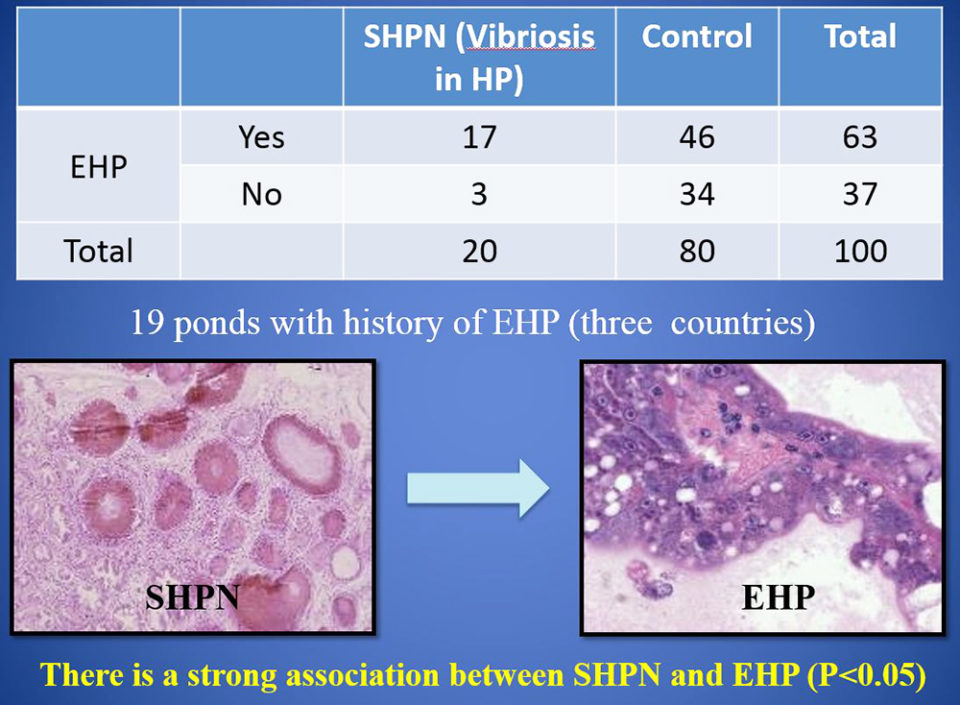
En el estudio de control de casos (EHP y SHPN a nivel de granja), durante el período 2015-2016, se analizaron los registros de 100 camarones juveniles de P. vannamei de 19 estanques de crecimiento en granjas del sudeste asiático con antecedentes de EHP. Nuestros datos muestran una fuerte asociación entre los casos de SHPN y camarones infectados con EHP. Y la frecuencia de SHPN fue mayor en animales con EHP que en aquellos camarones sin EHP.
Perspectivas
La fuerte asociación encontrada entre los casos de SHPN y EHP sugiere que EHP aumenta la susceptibilidad del camarón a la infección por bacterias Vibrio – patógenos oportunistas conocidos que causan enfermedad cuando la salud del camarón está comprometida. La infección por EHP perturba las células de los túbulos del hepatopancreas y permite al Vibrio spp. ya presentes el colonizar las células desprendidas y la membrana basal expuesta.
Utilizando dos métodos independientes, nuestro estudio demostró que los camarones blancos del Pacífico infectados con EHP estaban co-infectados con AHPND y SHPN. Los efectos significativos de estas co-infecciones se explican muy probablemente por las acciones sinérgicas de los patógenos microsporidianos y bacterianos en el tejido del hepatopancreas. A través de sus acciones combinadas, la co-infección de VPAHPND y EHP aumenta dramáticamente el daño al hepatopancreas, hasta el punto de causar la falla y morbilidad totales del tejido.
Nuestros resultados pueden ayudar a explicar los patrones observados de aparición de brotes de enfermedades en los países productores de camarón en todo el mundo. Por ejemplo, países de Asia Sudoriental – como China, Vietnam, Tailandia y Malasia – que han sufrido brotes de EHP durante la última década, también sufrieron brotes de AHPND años después. Otros países como Indonesia e India han reportado recientemente la presencia de EHP, pero aún no han experimentado brotes de AHPND.
Sin embargo, en Indonesia una enfermedad emergente conocida como síndrome de heces blancas (WFS) parece ser debida a la co-infección de EHP con otros Vibrios spp. oportunistas que causan SHPN. Del mismo modo, en la India, el síndrome de mortalidad en marcha (RMS) se ha reportado recientemente, con los animales afectados teniendo lesiones graves del hepatopáncreas.
El desarrollo de medidas para prevenir EHP o para tratar los estanques afectados podría reducir considerablemente las pérdidas de producción de camarón de cultivo, y fomentamos esta investigación.
Referencias disponibles del primer autor.
Now that you've reached the end of the article ...
… please consider supporting GSA’s mission to advance responsible seafood practices through education, advocacy and third-party assurances. The Advocate aims to document the evolution of responsible seafood practices and share the expansive knowledge of our vast network of contributors.
By becoming a Global Seafood Alliance member, you’re ensuring that all of the pre-competitive work we do through member benefits, resources and events can continue. Individual membership costs just $50 a year.
Not a GSA member? Join us.
Authors
-

Luis Fernando Aranguren, Ph.D.
School of Animal and Comparative Biomedical Sciences
University of Arizona
Aquaculture Pathology Laboratory
Tucson, AZ 85721 USA[117,100,101,46,97,110,111,122,105,114,97,46,108,105,97,109,101,64,117,103,110,97,114,97,102,108]
-

Jee Eun Han, D.V.M. Ph.D.
CJ CheilJedang Feed & Livestock Research Institute
CJ Blossom Park
Suwon-si, Gyeonggi-do, Korea[109,111,99,46,108,105,97,109,103,64,51,50,50,49,101,106,110,97,104]
-

Kathy F.J. Tang, Ph.D.
School of Animal and Comparative Biomedical Sciences
University of Arizona
Tucson, AZ 85721 USA[117,100,101,46,97,110,111,122,105,114,97,46,108,105,97,109,101,64,117,121,106,103,110,101,102]
Tagged With
Related Posts

Health & Welfare
Cuatro cepas de AHPND identificadas en granjas de camarón de América Latina
Se conocen dos genes de virulencia que codifican una toxina binaria de Photorhabdus relacionada con insectos que causa la enfermedad de necrosis hepatopancreática aguda en camarones. Las patogenicidades de estas cepas de V. campbellii fueron evaluadas mediante infección de laboratorio y posterior examen histológico en camarones P. vannamei.

Health & Welfare
Probióticos benefician al camarón blanco del Pacífico desafiado con AHPND
Un estudio fue llevado a cabo para medir los efectos de probióticos comerciales en camarón blanco del Pacífico en un modelo de desafío a AHPND estandarizado bajo condiciones controladas de laboratorio. Los resultados muestran que los tratamientos de probióticos por sí mismos tienen efectos beneficiosos, como una mayor supervivencia y signos histológicos de regeneración de hepatopáncreas.

Health & Welfare
Herramienta diagnóstica no-invasiva desarrollada para la enfermedad EMS del camarón
La presencia de AHPND-Vibrio parahaemolyticus puede ser detectada tanto en muestras de ADN fecal como en caldo bacteriano enriquecido con muestras de caldo de enriquecimiento que muestran mayor sensibilidad.

Intelligence
Podemos crecer un mejor camarón, y de mejores maneras
El reciente Simposio Centroamericano de Acuicultura en Choluteca, Honduras, reunió a más de 600 participantes para discutir temas de la industria y sus perspectivas. La atención se centró en enfermedades del camarón y sus impactos en la producción, así como en alternativas prácticas.


