Los resultados mostraron una supervivencia, crecimiento y eficiencia de alimentación adecuadas con reutilización de agua, cero descarga

La cría de camarones en Brasil ha experimentado una serie de avances tecnológicos, impulsados principalmente por la búsqueda de una mayor productividad de la granja de camarones. A principios de la década de 1980, las granjas pioneras adoptaron un régimen semi-extensivo, caracterizado por una baja densidad de población (1 a 3 camarones por metro cuadrado) y fertilización orgánica para el desarrollo de alimentos bentónicos, lo que resultaba en rendimientos entre 50 y 200 kg/ha/cosecha. Desde mediados de la década de 1990 en adelante, con la disponibilidad de postlarvas de camarones blancos del Pacífico (Litopenaeus vannamei) y alimentos compuestos industriales, se introdujeron prácticas semi-intensivas. Estos se caracterizaron por un mayor control del manejo del alimento mediante el uso de bandejas de alimentación y densidades de hasta 30 camarones por metro cuadrado, lo que dio como resultado rendimientos cercanos a 1.500 kg/ha/cultivo. A fines de la década de 2000, los productores implementaron prácticas más intensivas, la energía eléctrica fue llevada a las granjas para permitir el uso de aireación mecánica y se comenzaron a utilizar estanques de tierra con áreas de hasta 5 ha. En 2003, las densidades podían superar los 50 camarones por metro cuadrado, con rendimientos cercanos a los 4.000 kg/ha/cosecha.
Actualmente se están implementando tecnologías de producción superintensivas en algunas granjas en la parte noreste de Brasil. A diferencia de los estanques de tierra intensivos, estos sistemas operan para lograr un equilibrio entre la alta productividad del camarón, los parámetros de calidad del agua, el intercambio de agua reducido y una mayor bioseguridad. Los estanques utilizan áreas cuadradas o rectangulares entre 2.500 y 4.000 metros cuadrados, profundidades entre 1,8 y 3,0 metros, con fondos revestidos con geomembranas de polietileno de alta densidad (HDPE) y equipados con desagües centrales. Puede haber cuencas para la reutilización del agua, con cubierta de invernadero, estructura de PVC, madera o metal galvanizado, cubiertas con película semitransparente u opaca. Los camarones se alimentan varias veces al día mediante distribución manual o usando bandejas de alimentación, se utiliza una alta tasa de aireación mecánica (20 a 30 hp/ha), las densidades iniciales de población varían entre 120 y 300 camarones por metro cuadrado, y los rendimientos pueden alcanzar hasta 25.000 kg/ha/cosecha.
Estudios recientes sobre sistemas superintensivos han convergido a un sistema híbrido que combina la recirculación de agua (sistema de recirculación acuícola, RAS), la presencia de flóculos microbianos y cero descargas de agua. El principio básico de RAS es el tratamiento del agua de descarga a través de una serie de procesos, que pueden incluir filtración física y mecánica, biofiltración, desinfección y oxigenación antes de devolver el agua tratada al sistema de cultivo. Este artículo presenta los resultados de tres ensayos superintensivos con juveniles de L. vannamei llevados a cabo en las instalaciones de investigación de LABOMAR, utilizando tanques circulares experimentales, operados con un mínimo intercambio de agua o en un sistema híbrido con reutilización total de agua. Específicamente, el estudio determinó el rendimiento del camarón con respecto a la supervivencia final, el peso corporal, el consumo de alimento, la relación de conversión de alimento y el rendimiento en respuesta al régimen de intercambio de agua, la densidad de población y el alimento utilizado.
Nota del editor: Este artículo resume la siguiente investigación reciente de pregrado en la Universidade Federal do Ceará, Fortaleza, CE, Brasil: 1) Soares, A.N. 2018. Avaliação de ração comercial para o cultivo super-intensivo de juvenis do camarão branco do Pacífico, Litopenaeus vannamei, com um mínimo de troca de água. Tesis de Licenciatura en Ingeniería Pesquera. Universidade Federal do Ceará, Fortaleza, CE, Brasil. 36 p .; y 2) Santos, I.B. 2019. Cultivo do camarão Litopenaeus vannamei en sistema híbrido super-intensivo, con cero descarga y reuso de água. Tesis de Licenciatura en Oceanografía. Universidade Federal do Ceará, Fortaleza, CE, Brasil. 34 p.
Configuración del estudio
El diseño utilizado en este estudio consistió en 25 tanques cilíndricos con un volumen utilizable de 6.37 a 7.96 metros cúbicos (área de 5.31 metros cuadrados x 1.20 a 1.50 metros de profundidad) y una estructura de acero galvanizado y lona de PVC. Los tanques se mantuvieron abiertos, semicubiertos con pantalla de sombra y película opaca/lechosa, equipados individualmente con una entrada y salida de agua separadas, aireación con una o dos mangueras porosas, alimentador automático y bandeja de alimentación para estimar indirectamente el consumo de alimento (Fig. 1) Los tanques de cultivo tienen dos líneas de conexión de agua, una para el suministro de agua reutilizada y otra para el drenaje de aguas residuales, conectadas a dos depósitos enterrados de 5 y 10 metros cúbicos. Estos depósitos reducen y oxidan la materia orgánica presente en el agua de descarga mediante desnitrificación, sedimentación, nitrificación y oxigenación intensa. El agua tratada va a otros dos depósitos de 20 metros cúbicos y luego se bombea a los tanques de cultivo.

Se realizaron tres ensayos consecutivos (1, 2 y 3), modificando los alimentos comerciales utilizados, la preparación del agua, el régimen de intercambio de agua, las densidades de población de camarones y los métodos de alimentación (Tabla 1). La preparación de los tanques para las pruebas comenzó lavando las paredes del tanque con agua y cloro. Posteriormente, los tanques fueron expuestos a la luz solar y luego enjuagados con agua salada para eliminar los desechos. Al día siguiente, los tanques se llenaron con agua estuarina, prefiltrada con un filtro de arena. En el ensayo 3, el agua se desinfectó con 5 ppm de hipoclorito de calcio.
Nunes, superintensivo, Tabla 1
| Características | Prueba 1 | Prueba 2 | Prueba 3 |
|---|---|---|---|
| Densidad inicial (camarones/m2) | 186 | 282 | 659 |
| Profundidad (volumen del tanque) | 1.20 m (6.37 m3) | 1.20 m (6.37 m3) | 1.50 m (7.56 m3) |
| Preparación de agua | Filtro de arena | Filtro de arena | Filtro de arena y cloro |
| Fertilización de agua | Alimento molido y melaza | Alimento molido y melaza | Simbiótico y melaza |
| Aireación | Manguera, un punto | Manguera, un punto | Manguera, dos puntos |
| Régimen de agua | Recambio mínimo | Recambio mínimo | RAS, reuso integral |
| Cobertura del tanque | Malla sombra 70% | Malla sombra 70% | Malla sombra y plástico |
| Manejo de alimento | Bandejas | Bandejas | Manual y mecánico |
| Frecuencia de alimentación | 4 veces al día | 4 veces al día | 20 veces, día y noche |
| Peso corporal inicial (g) | 1.74 ± 0.64 | 1.53 ± 0.33 | 1.32 ± 0.24 |
| Tiempo de cultivo (días) | 81 | 87 | 64 |
Antes de la siembra de camarones, el agua del tanque fue fertilizada para promover el crecimiento y el dominio de las bacterias heterotróficas y nitrificantes. El agua se fertilizó aplicando a cada tanque 8.8 gramos por metro cúbico de alimento para camarones molidos que contenía un mínimo de 35 por ciento de proteína cruda junto con 10 gramos por metro cúbico de melaza de caña de azúcar. En el ensayo 3, la melaza se usó en combinación con una preparación fermentada que consistía en residuos de arroz y levadura viva (simbiótica). Este procedimiento se repitió tres veces por semana durante el primer mes de cultivo de camarones. El material fermentado fue reemplazado por melaza de caña de azúcar desde el segundo mes de cultivo para mantener el color parduzco deseado del agua de cultivo, característica del dominio de las bacterias nitrificantes en el sistema (Fig. 2).

Los camarones se sembraron con un peso corporal inicial entre 1,3 y 1,7 gramos y a densidades de 186, 282 y 659 animales por metro cuadrado en los ensayos 1, 2 y 3, respectivamente. En todos los ensayos, los camarones fueron alimentados con alimentos comerciales hechos en Brasil. En los cultivos 1 y 2, el alimento se entregó cuatro veces al día, exclusivamente en bandejas de alimentación con un área de 707 cm cuadrados (30 cm de diámetro x 5,4 cm de altura), con una bandeja por tanque. El alimento se ofreció a las 7 a.m., 10 a.m., 1 p.m. y 4 p.m., y la ración diaria se dividió en 25, 15, 15 y 45 por ciento en los horarios respectivos.

En la prueba 3, los alimentos comerciales se entregaron de forma mecánica y manual. Durante el día, entre las 8 a.m. y las 4 p.m., los alimentos se entregaron utilizando alimentadores mecánicos y distribuyendo manualmente a intervalos de una hora. Por la noche, la alimentación se distribuía mecánicamente utilizando un dispositivo de alimentación automatizado programado para entregar alimentos cada hora. Las raciones diurnas y nocturnas representaban el 60 y el 40 por ciento del alimento total diario, respectivamente. Se colocó una bandeja de alimentación debajo de cada alimentador para controlar el consumo nocturno de alimento. Durante el día, se retiraron las bandejas de los tanques, se evaluó visualmente la cantidad de sobras y las bandejas se lavaron y se reemplazaron en los tanques.
En todas las pruebas, las raciones se ajustaron diariamente, suponiendo una disminución semanal de 0,5 por ciento en la supervivencia de camarones en todos los tanques de cultivo. Las comidas se ajustaron semanalmente, comenzando el séptimo día de cultivo. En cada sesión de muestreo, se pesó un total de 20 camarones por tanque en una escala de precisión para determinar el peso medio de la población. Hasta el próximo control de peso, el aumento de las raciones se realizó diariamente sobre la base del crecimiento diario promedio de camarones observado en la semana anterior, con una disminución de la supervivencia semanal del 0,5 por ciento.
La salinidad, el pH, la temperatura y el oxígeno disuelto se determinaron una vez al día a las 9 a.m. en todos los tanques. Los sólidos sedimentables (SS) se midieron tres veces por semana utilizando conos de Imhoff de 1.000 ml (Fig. 3). Se determinó la alcalinidad para la corrección con bicarbonato de sodio (NaHCO3). Se realizó una aplicación de 20 gramos por metro cúbico de NaHCO3 por cada aumento de 10 mg/L en la alcalinidad del agua.
Resultados y discusión
En los ensayos 1 y 2, el camarón logró una alta supervivencia final superior al 90 por ciento (Tabla 2). No hubo un efecto significativo del tipo de alimento utilizado en la supervivencia del camarón (P> 0,05). Aunque hubo un aumento en la densidad inicial de camarones del 52 por ciento entre los ensayos 1 y 2 (de 186 a 282 camarones por metro cuadrado, respectivamente), el aumento en la densidad no tuvo influencia en la supervivencia final de los camarones. La supervivencia promedio alcanzó valores muy cercanos, de 91,49 ± 5,07 y 91,65 ± 3,50 por ciento, respectivamente. Esto sugiere que no se excedió la capacidad de carga de los tanques. En el ensayo 3 con 659 camarones por metro cuadrado, hubo una reducción a 82,0 ± 7,0 por ciento en la supervivencia final. Sin embargo, no hubo influencia del tipo de alimento utilizado en la supervivencia del camarón (P> 0,05).
Nunes, superintensivo, Tabla 2
| Rendimiento zootécnico | Prueba 1 | Prueba 2 | Prueba 3 |
|---|---|---|---|
| Supervivencia final (%) | 91.49 ± 5.07 | 91.65 ± 3.50 | 82.00 ± 7.0 |
| Crecimiento semanal (g) | 0.89 ± 0.03 – 1.13 ± 0.19 | 0.82 ± 0.09 – 1.00 ± 0.04 | 1.17 ± 0.14 |
| Peso corporal final (g) | 12.08 ± 0.22 – 14.76 ± 2.20 | 11.77 ± 1.11 – 13.95 ± 0.50 | 11.45 ± 1.27 – 12.98 ± 0.86 |
| Productividad final (g/m2) | 2,227 ± 177 | 2,982 ± 266 – 3,573 ± 93 | 6,526 ± 438 |
| Consumo de alimento (g/ camarones) | 18.5 ± 0.74 – 20.1 ± 0.76 | 17.6 ± 1.17 – 19.8 ± 1.06 | 14.0 ± 1.2 |
| FCR | 1.85 ± 0.19 | 1.85 ± 0.11 | 1.63 ± 0.08 |

El rendimiento final del camarón aumentó linealmente en función de la densidad inicial del camarón. Con 186 camarones por metro cuadrado, la productividad alcanzó 2.227 ± 177 gramos por metro cuadrado. Con una densidad de población de 282 camarones por metro cuadrado, el rendimiento final varió de 2.982 ± 266 a 3.573 ± 93 gramos por metro cuadrado, y el alimento tuvo un efecto estadísticamente significativo sobre este parámetro. En la prueba 3, el rendimiento promedio fue de 6.526 ± 438 gramos por metro cuadrado, pero se obtuvieron valores promedio de 6.892 ± 314 gramos por metro cuadrado para uno de los alimentos utilizados.
En el ensayo 1, el crecimiento semanal del camarón varió de 0,89 ± 0,03 a 1,13 ± 0,19 gramos, mientras que en el ensayo 2 los valores fueron más bajos, entre 0.82 ± 0.09 y 1,00 ± 0,04 gramos. El crecimiento del camarón se vio significativamente afectado por el tipo de alimento utilizado. Aunque se puede especular que la reducción en el crecimiento semanal en los cultivos 1 y 2 se debió al aumento en la densidad inicial de camarones, en 659 camarones por metro cuadrado el crecimiento aumentó a un promedio de 1,17 ± 0,14 gramos. Lo más probable es que las diferentes tasas de crecimiento observadas fueran el resultado de las características operativas de cada cultivo, en particular el manejo del alimento y el tipo de alimento utilizado.
No fue posible observar grandes cambios en los parámetros de calidad del agua de los diferentes ensayos que podrían justificar las diferencias en el crecimiento del camarón. Los promedios observados (± desviación estándar) para temperatura, salinidad y pH en los cultivos 1 y 2 fueron 29,1 ± 0,6 grados-C (n = 1.725) y 30,6 ± 1,0 grados-C (n = 1,699), 36 ± 5, 3 gramos/L (n = 1.725) y 41 ± 1,8 gramos/L (n = 1.699), 7,65 ± 0,65 (n = 1.725) y 7,45 ± 0,34 (n = 1.700), respectivamente. En el ensayo 2, el oxígeno disuelto (OD) y los sólidos sedimentables (SS) alcanzaron un promedio de 4,71 ± 0,62 mg/L (n = 1.700) y 2,7 ± 1,8 mL/L (n = 1.725). Comparativamente, en el ensayo 3, la temperatura, la salinidad, el pH, el oxígeno disuelto y el SS alcanzaron un promedio de 29,6 ± 1,3 grados-C (n = 1.125), 42 ± 2 g/L (n = 1.125), 7,24 ± 0,58 (n = 1.125), 3,75 ± 0,62 mg/L (n = 325) y 1,4 ± 1,3 mL/L (n = 450). Sin embargo, en este cultivo, hubo caídas progresivas en el pH y la alcalinidad del agua durante todo el experimento, controladas por la aplicación de bicarbonato de sodio para mantener el pH cerca de la neutralidad, con niveles de alcalinidad superiores a 100 mg/L de CaCO3.
El peso corporal final de los camarones estuvo significativamente influenciado por el tipo de alimento utilizado en todas las densidades utilizadas. La diferencia en el ensayo 1 (12,08 ± 0,22 – 14,76 ± 2,20 gramos) entre los promedios mínimos y máximos observados fue de 2,68 gramos. En la prueba 2, la diferencia (11,77 ± 1,11 – 13,95 ± 0,50 gramos) alcanzó 2,18 gramos, y 1,53 gramos en la prueba 3 (11,45 ± 1,27 – 12,98 ± 0,86). Estos resultados muestran diferencias en el contenido nutricional y el valor biológico de los alimentos para camarones criados bajo altas densidades de población. Esto queda claro a partir de un análisis de la progresión del aumento de peso corporal de los camarones. Después de 26 días de cultivo, los camarones almacenados a 186 animales/m2 alcanzaron un promedio de 4,48 gramos, mientras que a 282 animales por metro cuadrado, fueron 3,10 gramos. Aunque el peso corporal inicial de los camarones en el cultivo 1 fue un 14 por ciento más alto (1,74 ± 0,64 gramos) que en el cultivo 2 (1,53 ± 0,33 gramos), las diferencias después de casi un mes de cultivo aumentaron al 45 por ciento. Sin embargo, en el cultivo 3, a 659 animales por metro cuadrado, el camarón alcanzó un promedio de 5,13 ± 0,13 gramos para el día 29 de cultivo.
Una correlación entre los días de cultivo y todos los pesos corporales de camarones recolectados a lo largo de los ensayos indica que debajo de 659 camarones por metro cuadrado, la progresión estimada en el aumento de peso se mantiene por encima de las otras densidades (Fig. 5).
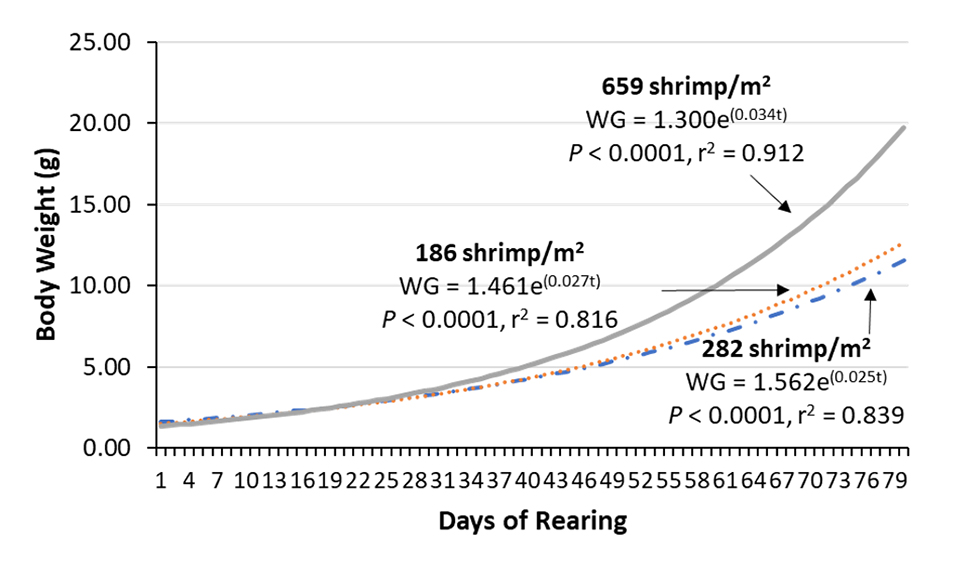
El consumo aparente de alimentos por los camarones varió entre los ensayos 1 y 2, y entre los alimentos utilizados. Se esperaban estas variaciones, dadas las diferencias observadas en el peso corporal de los camarones durante todo el período de cultivo. Sin embargo, en el ensayo 3 hubo una disminución significativa del consumo aparente de alimento. Esto se debió al mayor monitoreo del consumo de alimento, una mayor restricción impuesta en la tabla de alimentación, y también debido a la mayor frecuencia de alimentación adoptada. Estos procedimientos permitieron reducir el FCR de 1,85 en las pruebas 1 y 2 a 1,63 en la prueba 3, sin ninguna pérdida en el rendimiento del crecimiento.
Conclusiones
A través de los resultados de este estudio, fue posible verificar que los juveniles de L. vannamei tienen una supervivencia, crecimiento y eficiencia alimentaria adecuados cuando se cultivan a alta densidad, utilizando un intercambio mínimo de agua o una reutilización total del agua mediante la recirculación. El aumento en la densidad de población inicial de 186 a 282 camarones por metro cuadrado no tuvo un efecto perjudicial en el rendimiento zootécnico de los animales. Bajo estas densidades y en condiciones experimentales, L. vannamei logra una supervivencia superior al 90 por ciento, un crecimiento semanal entre 0,8 y 1,1 g, y una productividad entre 2,2 y 3,0 kg por metro cuadrado.
Los camarones también pudieron soportar densidades de población aún mayores, a 659 camarones por metro cuadrado, sin comprometer su supervivencia y crecimiento. Esta densidad resultó en supervivencia, crecimiento y rendimiento final equivalente al 82 por ciento, 1,32 gramos/semana y 6,5 kg por metro cuadrado, respectivamente. A esta densidad de población, los camarones se cultivaron en un sistema híbrido que funcionaba con recirculación continua de agua para permitir la sedimentación y la eliminación de sólidos en suspensión. Esto permitió una estabilidad en la concentración de compuestos nitrogenados, y no fue necesario mantener el sistema en un régimen heterotrófico o con dominancia de biofloc.
Ahora que Ud. ha terminado de leer el artículo ...
… esperamos que considere apoyar nuestra misión de documentar la evolución de la industria de acuícola global y compartir nuestra vasta red de conocimiento en expansión de los contribuyentes cada semana.
Al convertirse en miembro de la Global Aquaculture Alliance, se asegura de que todo el trabajo pre-competitivo que realizamos a través de los beneficios, recursos y eventos de los miembros (la Academia, The Advocate, GAA Films, GOAL, MyGAA) pueda continuar. Una membresía individual cuesta solo $ 50 al año.
Authors
-
Alberto J.P. Nunes, Ph.D.
Corresponding author
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil[32,114,98,46,99,102,117,64,115,101,110,117,110,46,111,116,114,101,98,108,97]
-
Allan Guedes Coutinho
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Daniel Camelo de Sena
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Lucas Alves Rufino
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Severino Campos Oliveira Neto
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Hassan Sabry Neto, Ph.D.
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Isaac Basílio dos Santos
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil -
Artur Nepomuceno Soares
LABOMAR – Instituto de Ciências do Mar
Universidade Federal do Ceará
Av. da Abolição, 3207 – Meireles, Fortaleza, Ceará 60.165-081 Brazil
Tagged With
Related Posts

Innovation & Investment
En la GOAL, un vistazo a los futuros potenciales de la acuacultura
En la conferencia anual GOAL de la Global Aquaculture Alliance en Guayaquil, Ecuador, temas desconocidos dieron a los líderes de la industria acuícola algo para reflexionar.

Aquafeeds
Análisis de la hidro-estabilidad de los alimentos de camarón
La integridad física y la lixiviación de nutrientes de los alimentos acuícolas para camarón son aspectos importantes en su control de calidad. La estabilidad en el agua de los alimentos de camarón se evalúa a menudo de diversas maneras subjetivas. Este procedimiento analítico proporciona una línea de base para que el fabricante de alimentos acuáticos evalúe la calidad del producto.

Aquafeeds
Sistemas de RAS de biofloc y agua clara: una comparación
En este estudio se compararon dos tipos de sistemas de cultivo de camarón bajo techo: RAS de aguas claras y sistemas de biofloc. El RAS de aguas claras tuvo la ventaja en la calidad del agua, y el camarón en el tratamiento biofloc tuvo una mayor conversión de alimento.

Aquafeeds
Sustitución de la harina de pescado por DFB en dietas de pámpano
Un estudio evaluó la inclusión de biomasa bacteriana fermentada seca como un reemplazo para la harina de pescado en cuatro dietas prácticas para juveniles de pámpano de Florida. No hubo diferencias significativas en el peso final, supervivencia, FCR o el coeficiente de crecimiento de la unidad térmica.



