Resultados del estudio útiles como método de selección inicial

El protozoario Paramoeba sp. (sinónimo de Neoparamoeba sp.) es omnipresente y normalmente vive libre en aguas marinas, y es el parásito protozoario ameboide más patógeno en peces cultivados. La especie P. perurans coloniza las branquias y da como resultado la enfermedad de las branquias amebianas (AGD) en salmónidos criados en granjas y, en particular, afecta a la industria del salmón del Atlántico en Tasmania, con pérdidas típicas del 10 al 20 por ciento de la producción. Hasta el momento, la AGD se ha registrado en 15 especies de peces de 11 géneros diferentes, y en la infección por P. perurans en el pescado se producen reacciones celulares proliferativas en las branquias, que incluyen hiperplasia epitelial, hipertrofia, edema y formación de vesículas interlamelares como manchas y placas blancas mucoides en la superficie de las branquias.
La evaluación patológica general de las branquias se ha utilizado ampliamente para el diagnóstico de AGD, pero se recomienda un examen histológico posterior para mejorar la precisión diagnóstica. Además, los métodos de diagnóstico molecular basados en el ensayo de PCR convencional que se dirige a la secuencia del rRNA (SSU rRNA) de la subunidad pequeña están disponibles para el diagnóstico de la AGD.
También se han reportado varias especies de Paramoeba en algunas especies de crustáceos y equinodermos, como langostas, cangrejos y erizos de mar. En estos huéspedes, las infecciones graves se asociaron con la muerte del huésped, lo que resultó en pérdidas económicas significativas. Las infecciones también se notificaron en moluscos bivalvos, como los mejillones, pero se consideró que tenían más probabilidades de ser reservorios ambientales potenciales para este protozoo.
Este artículo – adaptado y resumido de la publicación original – es el primer informe de este parásito protozoario ameboide en el camarón blanco del Pacífico (Litopenaeus vannamei). Este trabajo fue apoyado por la subvención de la Fundación Nacional de Investigación de Corea (NRF) financiada por el gobierno de Corea (MSIT) (número de concesión NRF-2018R1C1B5086350).
Configuración del estudio
Camarones del Pacífico adultos (peso promedio 30 gramos) de un criadero anónimo de camarones en América del Norte mostraron una disminución del apetito, letargo y dificultad respiratoria. La mortalidad acumulada fue de 62.75 por ciento a los 120 días después de la siembra, y los camarones enfermos tenían branquias negras, laminillas faltantes y caparazón erosionado (ver la imagen de arriba). De estos datos, sospechamos una infección por hongos causada por especies de Fusarium, que se ha reportado previamente como el agente causante de la enfermedad de las branquias negras en crustáceos, como langostinos, camarones y langostas. Sin embargo, se observaron parásitos protozoarios amebianos mediante la observación directa de un montaje húmedo (Fig. 1). Las muestras de camarones moribundos se recolectaron a intervalos irregulares, se fijaron en el fijador AFA de Davidson o en un 95 por ciento de etanol, y se examinaron posteriormente por histopatología, PCR e ISH.
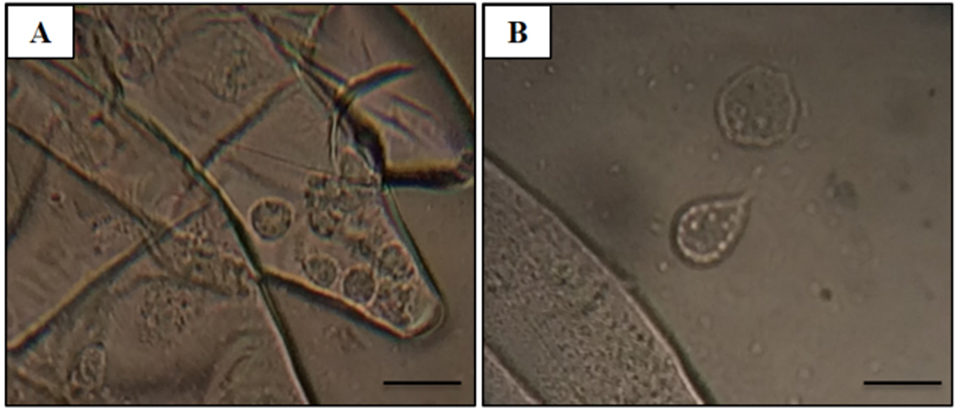
Para información adicional y detallada sobre el muestreo de camarones, el examen histopatológico y el análisis de secuencia, el ensayo de PCR y la hibridación in situ (ISH), consulte la publicación original.
Resultados y discusión: examen histopatológico (H&E)
El hallazgo más significativo en el examen microscópico de las muestras estudiadas fue la presencia de un parásito amebiano. La infestación por este parásito se encontró principalmente en las branquias, con grado de gravedad G4 (Figs. 2A – C), y se observó hiperplasia extensa, puente de laminillas y formación de espacios interlamelares. Según el productor, letargo, anoxia y, eventualmente, la muerte se ha visto en camarones infectados, y esto puede estar asociado con el daño a las branquias (órganos respiratorios). La figura 2A muestra el núcleo de la ameba con un núcleo anfifílico rodeado por un anillo basófilo irregular y el parasoma con el citoplasma eosinofílico y vacuolas, lo que indica que la ameba está estrechamente relacionada con los miembros del orden Dactylopodida, y tal vez el género Paramoeba, según Sühnel. et al. (2014).
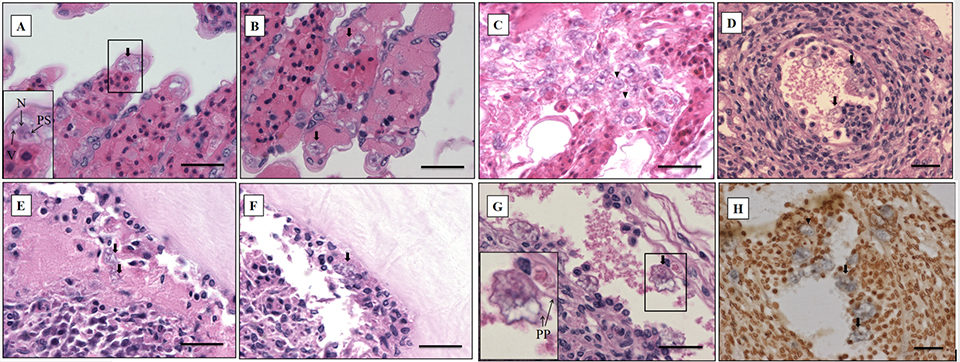
Además, se observaron predominantemente formas de trofozoítos aplanadas e irregulares con radiación de pseudópodos (aproximadamente de 25 a 30 µm de diámetro). La presencia de pseudópodos digitados, la falta de quistes (menos de 10 µm de diámetro) y el hábitat marino también identifican a la ameba como del género Paramoeba, según Kent et al. (1988). Estos parásitos amebianos también se observaron en otros órganos, como la glándula de la antena, el órgano linfoide, el epitelio cuticular y el subcutis de los apéndices y el tejido conectivo que rodea el cordón nervioso ventral de las muestras analizadas, con grado de gravedad G1 a G4 (Figs. 2D– SOL).
Ensayo de PCR y análisis de secuencia
Los amplicones fuertes (un amplicón es un fragmento de ADN o ARN que es la fuente y / o el producto de los eventos de amplificación o replicación) se detectaron en el camarón analizado (cinco muestras representativas) mediante el ensayo de PCR dirigido a la secuencia del ARNr del SSU (Fig. 3). Los resultados mostraron que la secuencia de nucleótidos era 100 por ciento idéntica a las secuencias de Paramoeba sp. (Neoparamoeba sp.) de varias especies de crustáceos marinos y equinodermos. Y no hubo reacción cruzada con el ADN genómico de los camarones L. vannamei y otros camarones (P. monodon, P. indicus, L. stylirostris y M. rosenbergii), poliquetos, calamares y Artemia spp., o con otros parásitos de los camarones por la prueba de especificidad.
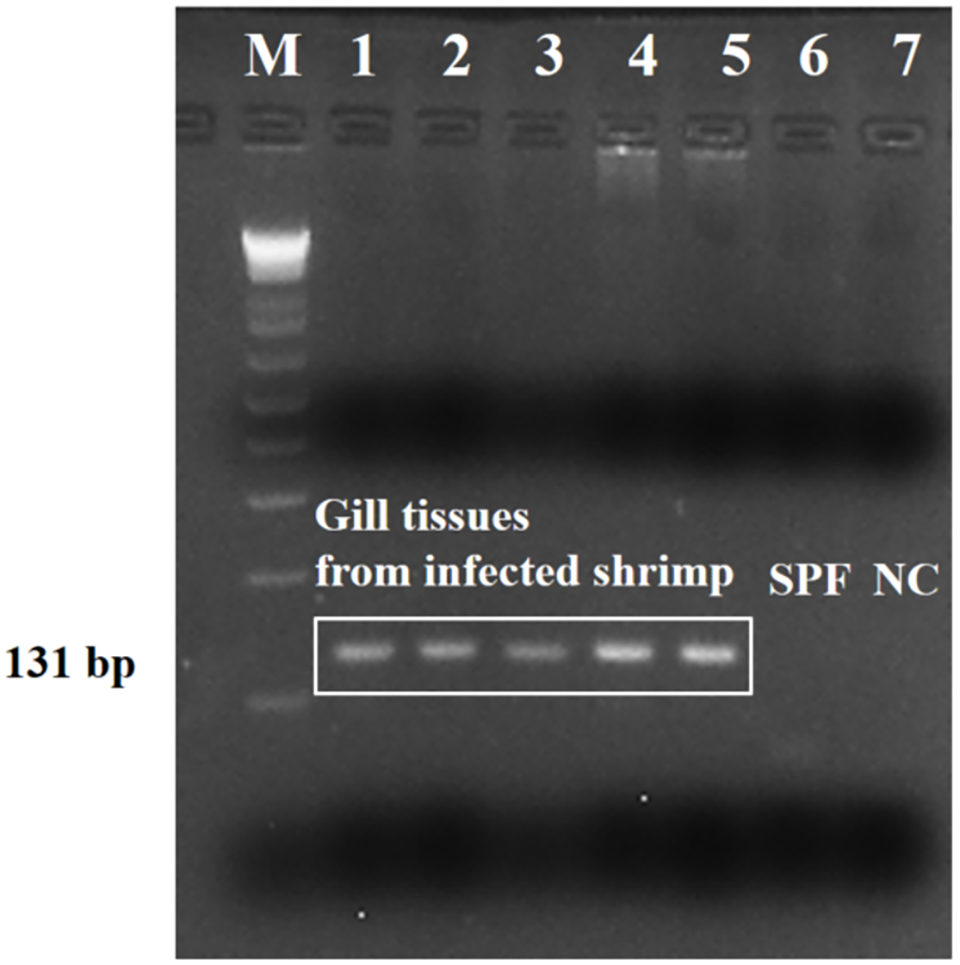
También realizamos un estudio filogenético para investigar la relación entre las especies identificadas como tipo-Paramoeba sp. de camarones y otras especies de amebas. En el árbol filogenético resultante, la secuencia del ARNr del SSU de la especie tipo-Paramoeba se agrupó junto con secuencias del orden Dactylopodida, especialmente la familia Paramoebidae.
Hibridación in situ
El método ISH también se puede utilizar para determinar los agentes etiológicos de la infección por protozoos. Para ISH, la sonda del gen tipo Paramoebase generó a partir de la secuencia de ARNu del SSU de los camarones infectados por la ameba, y esta se hibridó con las células amebianas en la muestra representativa (Fig. 2H), correspondiente a los resultados histopatológicos. La sonda parece ser muy específica y no se observó reacción en ninguno de los tejidos preparados a partir de camarones SPF (datos no mostrados).
Hasta ahora, el parásito protozoario ameboide Paramoeba sp. se ha reportado en varios crustáceos marinos, incluyendo la langosta Americana y cangrejos, pero no en el camarón cultivado. Este estudio es el primer informe de infección por el parásito prebozoico amebiano tipo-Paramoeba e sp. en las branquias de L. vannamei cultivado en un criadero anónimo en América del Norte. Es muy probable que la infección por amebas se deba a factores de estrés, como el aumento de la temperatura del agua y / o altas salinidades, combinadas con altas densidades de animales en estanques, lo que proporciona una ventaja a este protozoo naturalmente presente en el ambiente marino. Según los productores, la salinidad había caído de 34 a 10 ppt debido a problemas con el equipo mecánico, por lo que es probable que el estrés resultante haya provocado la infestación del parásito en los camarones.
Perspectivas
Los camarones infectados con la ameba mostraron una disminución del apetito, letargo, dificultad respiratoria, caparazones erosionados y branquias ennegrecidas. Bajo el microscopio, las características histopatológicas incluyeron la morfología típica de los protozoos amebianos que presentan endoplasmas granulares con vacuolas, núcleos, parasomas y ectoplasmas con pseudópodos. Estas características sugieren que el parásito está relacionado con el orden Dactylopodida, probablemente una especie de Paramoeba y esto se confirmó mediante el análisis de secuencia de ARNr del SSU, el ensayo de PCR y la hibridación in situ (ISH).
En el camarón, la infección por amebas ha resultado en una mortalidad significativa y pérdidas económicas asociadas. Por lo tanto, los ensayos de diagnóstico de ISH y PCR desarrollados en este estudio pueden proporcionar datos informativos para los productores de camarón y pueden utilizarse como los métodos de selección inicial para el protozoo ameboide en el camarón.
Este estudio proporciona datos informativos a los productores de camarón y los ayuda a monitorear las infecciones por amebas en granjas camaroneras. En los camarones examinados, los parásitos tienen características histológicas de Paramoeba sp., pero no se detectaron bandas de PCR para los cebadores generados a partir de P. perurans, P. pemaquidensis o P. branchiphila spp. Por lo tanto, asumimos que podría ser una nueva especie de Paramoeba que infecta camarones. Se necesita trabajo adicional para diagnosticar la especie y desarrollar los métodos de diagnóstico específicos de la especie para amebas que infectan camarones de granja.
Referencias disponibles del primer autor o de la publicación original.
Ahora que Ud. ha terminado de leer el artículo ...
… esperamos que considere apoyar nuestra misión de documentar la evolución de la industria de acuícola global y compartir nuestra vasta red de conocimiento en expansión de los contribuyentes cada semana.
Al convertirse en miembro de la Global Aquaculture Alliance, se asegura de que todo el trabajo pre-competitivo que realizamos a través de los beneficios, recursos y eventos de los miembros (la Academia, The Advocate, GAA Films, GOAL, MyGAA) pueda continuar. Una membresía individual cuesta solo $ 50 al año.
Authors
-

Jee Eun Han, DVM, Ph.D.
Laboratory of Aquatic Biomedicine
College of Veterinary Medicine
Kyungpook National University
Daegu 41566, Korea[32,109,111,99,46,108,105,97,109,103,64,51,50,50,49,101,106,110,97,104]
-
Ji Hyung Kim, Ph.D.
Senior researcher
Infectious Disease Research Center
Korea Research Institute of Bioscience & Biotechnology (KRIBB)
125 Gwahak-ro, Yuseong-gu, Daejeon 34141, Republic of Korea -
Kyeong Yeon Kim
Laboratory of Aquatic Biomedicine
College of Veterinary Medicine
Kyungpook National University
Daegu 41566, Korea -
Young Seo Lee
Laboratory of Aquatic Biomedicine
College of Veterinary Medicine
Kyungpook National University
Daegu 41566, Korea
Tagged With
Related Posts

Responsibility
Abordando la inocuidad en la cadena de suministro de tilapia de América Latina
En la última década, la experiencia adquirida por muchos productores de tilapia combinada con programas eficaces implementados por los gobiernos locales ha mejorado significativamente la producción de tilapia en varios países de América Latina como Colombia, México, Ecuador y otros importantes productores de tilapia de la región.

Health & Welfare
Científicos de salmón colaboran en la nueva iniciativa de salud global QASH
Un esfuerzo de cooperación entre científicos de salmón en Noruega, Escocia, Chile y Canadá apunta a desarrollar una herramienta aplicable a nivel mundial para ayudar a la gestión y certificación de granjas de salmón.
Innovation & Investment
Juntos es mejor: las alianzas impulsan la innovación en los principales laboratorios
Los laboratorios con asociaciones industriales están haciendo que la acuacultura sea más innovadora, eficiente y responsable. Estas colaboraciones ofrecen acceso a experticia, instalaciones y financiamiento para fomentar la industria y mejorar la inocuidad alimentaria mundial.

Intelligence
La producción actual, desafíos y el futuro del cultivo del camarón
En el Simposio de Acuacultura de Guatemala en Antigua, el enfoque fue el cultivo de camarón en la región: producción, nutrición, gestión de la salud y mercados.



