Para diagnósticos de rutina y detección de infecciones de bajo grado

El microsporidio Enterocytozoon hepatopenaei(EHP) infecta a los camarones peneidos y se ha considerado una amenaza crítica para la acuacultura del camarón, causando graves pérdidas económicas en las granjas camaroneras de varios países asiáticos. Los órganos diana incluyen el hepatopáncreas y el intestino medio, por lo que la infección por EHP puede afectar la función digestiva y de absorción, lo que produce un retraso en el crecimiento. Los camarones podrían infectarse con EHP por canibalismo o alimentándose de alimentos vivos contaminados con EHP.
Métodos de diagnóstico de EHP dirigidos a la secuencia SSU ARNr
Se han desarrollado varios métodos de diagnóstico de EHP basados en la subunidad pequeña (SSU) ARNr, incluyendo PCR, qPCR, hibridación in situy ensayos de amplificación isotérmica mediada por vuelta. Sin embargo, las secuencias SSU ARNr no son muy específicas para la detección de microsporidios y los métodos de PCR basados en el SSU ARNr pueden generar falsos positivos en muestras que no son de camarón. Por ejemplo, la secuencia del SSU ARNr de EHP compartió una similitud del 90 por ciento con la de Enterospora cancerique infecta a los cangrejos marinos. Por lo tanto, se necesita un método de PCR más específico para los diagnósticos de EHP.
Nuevo método de diagnóstico de EHP dirigido al gen de β-tubulina de EHP
En consecuencia, desarrollamos un nuevo método de diagnóstico de EHP con dos conjuntos de cebadores diseñados en base a la secuencia del gen de la β-tubulina (GenBank No. KX842357, Tabla 1).
Han, detección de EHP, Tabla 1
| Nombre del cebador | Secuencia (5’ to 3’) | Tamaño de amplicón (bp) |
|---|---|---|
| β-tubulina 1er-paso PCR | ||
| EHP-618F | CAGCTGGTTGAAAATGCAAA | 618 |
| EHP-618R | GTGCAAAAATGCCTTTCGTT | 618 |
| β-tubulina 2do-paso PCR (anidado) | ||
| EHP-237F | GATATGCGCCTCTGTGTTCA | 237 |
| EHP-237R | TGTTTGGAATCCACTCGACA | 237 |
Se realizó una PCR de primer paso con los cebadores EHP-618F/R en las siguientes condiciones de ciclado: desnaturalización inicial a 94 grados-C durante 3 minutos, seguido de 35 ciclos de 94 grados-C durante 30 segundos, 58 grados-C durante 30 segundos y 72 grados-C durante 30 segundos, y una extensión final a 72 grados-C durante 7 minutos.
Luego, se realizó una PCR (anidada) de segundo paso con los cebadores internos EHP-237F/R en las siguientes condiciones de ciclado: desnaturalización inicial a 94 grados-C durante 3 minutos, seguido de 20 ciclos de 94 grados-C para 30 segundos, 58 grados-C durante 30 segundos y 72 grados-C durante 30 segundos, y una extensión final a 72 grados-C durante 7 minutos.
La PCR de segundo paso (anidada) es 100 veces más sensible que la PCR de primer paso (Fig. 1) y, por lo tanto, es adecuada para detectar una infección de EHP de bajo nivel.

Estudio de muestras de campo – ensayo de PCR de primer paso
Para comparar la sensibilidad en muestras de campo, aplicamos varias muestras de camarón infectadas con EHP (n = 22) recolectadas de países del sudeste asiático (Vietnam, India, Tailandia e Indonesia) y de camarón de salmuera artemia spp. positiva para EHP (n = 6; todos en la etapa adulta) determinado por una PCR de SSU ARNu de EHP (los productos de PCR corresponden al no. de acceso KP759285) al ensayo de PCR de primer paso. Después de la primera etapa de la PCR, se generaron amplicones de 618 pb a partir de todas las muestras de EHP (n = 22) de varias granjas de camarones en los países mencionados anteriormente (Fig. 2).
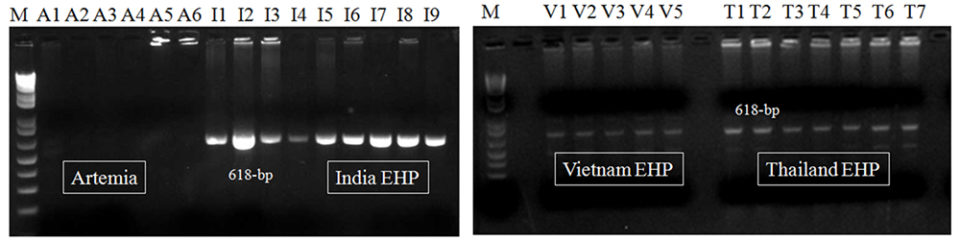
El ensayo de PCR de primer paso es simple y rápido. Sin embargo, no generó ningún amplicón a partir de las muestras de biomasa de artemia EHP positiva (n = 6), lo que podría deberse a las bajas cantidades de EHP presentes en estas muestras (Fig. 2).
Estudio de muestras de campo – ensayo de PCR de segundo paso (anidado)
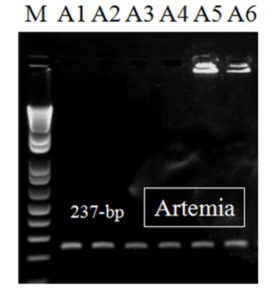
Después de la PCR (anidada) de segundo paso, se observó un fragmento de ADN de 237 bp en todas las muestras de EHP (n = 22), incluidas las de las muestras de biomasa de artemia (Fig. 3). Los resultados diagnósticos obtenidos por este método de PCR anidado son beneficiosos para el monitoreo de camarones con bajos niveles de infección por EHP. Además, este método es útil para detectar EHP en alimentos en vivo (como la artemia), que es importante en el campo porque los alimentos en vivo son un riesgo potencial de infección por EHP.
Perspectivas
En este estudio, desarrollamos un método de PCR anidado utilizando secuencias de genes de β-tubulina. Este nuevo método de PCR es específico al EHP y se puede utilizar en diagnósticos de rutina. Además, este método es útil para detectar una infección por EHP de bajo grado. Además, detectamos EHP en muestras de artemia mediante este método de PCR anidado. Sugiere la posibilidad de transferencia de EHP desde alimentos en vivo a los reproductores de camarón. En el campo, los camarones podrían infectarse con EHP alimentándose de alimentos vivos contaminados con EHP, como la artemia. Se requieren experimentos de laboratorio adicionales para determinar la infectividad de la artemia infectada por EHP en camarones.
Now that you've reached the end of the article ...
… please consider supporting GSA’s mission to advance responsible seafood practices through education, advocacy and third-party assurances. The Advocate aims to document the evolution of responsible seafood practices and share the expansive knowledge of our vast network of contributors.
By becoming a Global Seafood Alliance member, you’re ensuring that all of the pre-competitive work we do through member benefits, resources and events can continue. Individual membership costs just $50 a year.
Not a GSA member? Join us.
Authors
-

Jee Eun Han, DVM, Ph.D.
Laboratory of Aquatic Biomedicine
College of Veterinary Medicine
Kyungpook National University
Daegu 41566, Korea[32,109,111,99,46,108,105,97,109,103,64,51,50,50,49,101,106,110,97,104]
-

Kathy F.J. Tang, Ph.D.
Yellow Sea Fisheries Research Institute
Chinese Academy of Fishery Sciences
Qingdao 266071, China -

Ji Hyung Kim, Ph.D.
Infectious Disease Research Center
Korea Research Institute of Bioscience and Biotechnology
Daejeon 34141, Republic of Korea
Tagged With
Related Posts

Health & Welfare
Construyendo un mejor pre-criadero de camarones, parte 1
Los sistemas de pre-criadero de camarones ofrecen una oportunidad importante para aumentar los beneficios. Los pre-criaderos adecuadamente diseñados y operados son instalaciones altamente bioseguras para criar postlarvas a densidades muy altas. El objetivo es producir juveniles fuertes, sanos y uniformes con un potencial significativo de crecimiento compensatorio después de su transferencia para el crecimiento final en estanques.

Health & Welfare
EHP es un factor de riesgo para otras enfermedades del camarón
Desafíos de laboratorio y un estudio caso-control se utilizaron para determinar los efectos de la infección por EHP en dos enfermedades de Vibrio: necrosis hepatopancreática aguda (AHPND) y necrosis hepatopancreática séptica (SHPN).

Intelligence
La producción actual, desafíos y el futuro del cultivo del camarón
En el Simposio de Acuacultura de Guatemala en Antigua, el enfoque fue el cultivo de camarón en la región: producción, nutrición, gestión de la salud y mercados.
Health & Welfare
Enfermedad emergente: el Virus Iridiscente de Hemocitos de Camarón (SHIV)
SHIV es un nuevo virus del camarón blanco del Pacífico en la familia Iridoviridae. Los autores también desarrollaron un ensayo ISH y un método de PCR anidado para su detección específica.

