Fagos aislados evaluados como efectivos en el control de principal enfermedad del camarón cultivado, inhibiendo el crecimiento bacteriano

La enfermedad de necrosis hepatopancreática aguda (AHPND) es causada por una bacteria Vibrio (V. parahaemolyticus) que ha causado mortalidades sustanciales (hasta un 100 por ciento) en camarones peneidos cultivados afectados en varios países.
Esta enfermedad se informó por primera vez en China en 2009 y se produjeron brotes posteriores en Malasia, Tailandia, Filipinas, México y varios otros países de América Latina, y en 2017 también en Bangladesh y los Estados Unidos. Las pérdidas debidas a AHPND se han estimado en más de $ 1 mil millones por año. Por lo tanto, es importante desarrollar e implementar efectivamente medidas de control para evitar pérdidas catastróficas en la industria de cultivo de camarón.
Los bacteriófagos, comúnmente llamados fagos, son virus ubicuos que infectan bacterias y se pueden usar para controlar enfermedades infecciosas en humanos, animales y plantas. El nombre se basa en la palabra bacterias y el Griego phagein, que significa “devorar.”
Los fagos pueden replicarse dentro de las bacterias después de inyectar su genoma en la bacteria. Los fagos se han propuesto como un método alternativo ya que muestran una actividad bacteriolítica efectiva y poseen ventajas sobre los antibióticos convencionales: los fagos son naturales y son más comunes y diversos, y ampliamente distribuidos en el medio ambiente, incluido el agua de mar, y también son relativamente baratos. Los fagos se han utilizado durante muchos años como una alternativa a los antibióticos en varios países, y son un posible tratamiento contra las cepas resistentes a múltiples medicamentos de muchas bacterias.
Resultados de infectividad de fagos
Para el bacteriófago pVp-1, se analizó su infectividad en 22 cepas de Vibrio parahaemolyticus (abreviadas como VpAHPND) causantes de AHPND. Estos aislados bacterianos se obtuvieron del agua del estanque, las muestras de sedimentos y los estómagos de camarones afectados por AHPND/EMS en el sudeste de Asia y países de América Latina. Los cultivos puros se obtuvieron por formación de rayas en placas de agar de soja tríptico (TSA) NaCl al 2 por ciento. Este fago pudo infectar el 91 por ciento (20 cepas) del VpAHPND probado y demostró una fuerte actividad bacteriolítica contra 3 cepas altamente patógenas (Fig. 1).
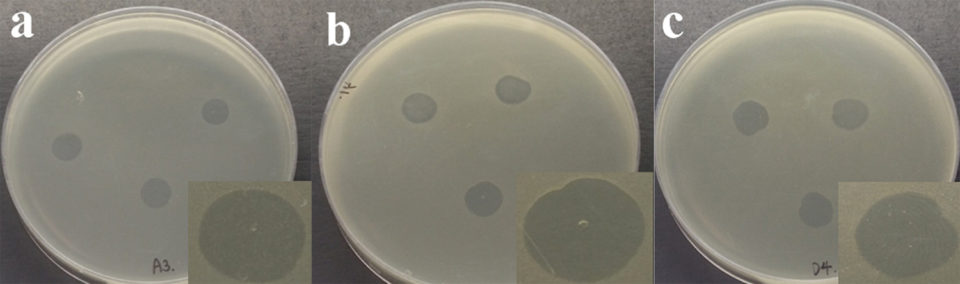
Evaluando la efectividad
Además, se evaluó su efectividad en los estudios de desafío en laboratorio con juveniles SPF (libre de patógenos específicos) de camarón blanco del Pacífico (Penaeus vannamei). Los animales de prueba (n = 96, peso promedio = 1,02 g) se mantuvieron en condiciones apropiadas (temperatura del agua 25 grados-C, salinidad 25 por ciento) y tres tanques se diseñaron para los controles.
El tanque 1 se designó como control negativo sin desafío bacteriano o tratamiento con fagos; el tanque 2 se designó como control de fagos con tratamiento de fagos mediante inmersión en baño (1,5 x 106 PFU/ml) y alimentación (1,5 x 108 PFU/camarones) usando gránulos (5 por ciento de peso corporal) que habían sido impregnados con la suspensión de fago, pero no desafiados bacterianamente Y el tanque 3 se designó como control positivo con un desafío bacteriano, pero no tratado con fago.
Para la prueba de desafío, se trataron camarones en varios tiempos (24, 6 y 1 hora antes del desafío bacteriano, y 1 hora después del desafío bacteriano) y se expusieron a V. parahaemolyticus 13-028/A3 (5,0 x 105 CFU/ml) durante 24 horas por el método de inmersión. Cada grupo se controló para detectar síntomas de infección y la mortalidad acumulada se registró diariamente durante cinco días después del desafío bacteriano.
De los resultados, los camarones tratados con pVp-1 mostraron una protección significativa, más del 25 por ciento (mortalidad máxima del 50 por ciento), mientras que los grupos de control positivo (no tratados con fago pVp-1, solo expuestos a VpAHPND) mostraron una mortalidad del 100 por ciento. Las características histopatológicas del hepatopáncreas del camarón se muestran en la Fig. 2.
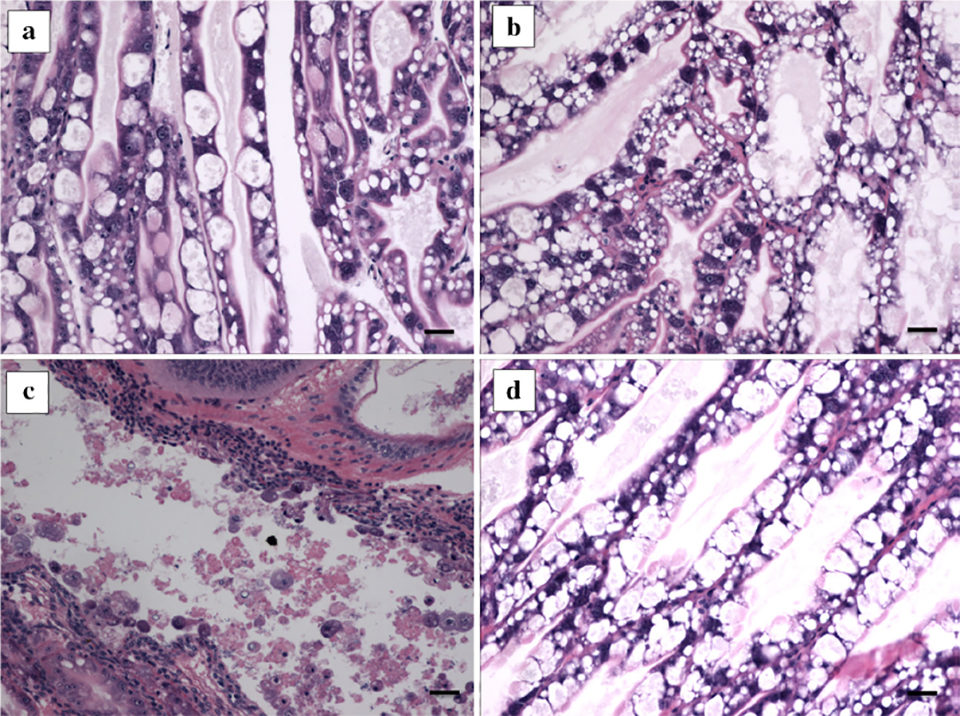
Las cepas de V. campbellii que llevan genes pirABvp de camarones enfermos fueron identificadas recientemente como agentes causantes de AHPND, y probamos estas cepas para el segundo bacteriófago, pVp-2, aislado de Penaeus vannamei. El fago pVp-2 lisaba eficazmente varios Vibrio parahaemolyticus (VpAHPND) y también Vibrio campbellii (VcAHPND) y formaba placas en placas TSA + (Fig. 3).
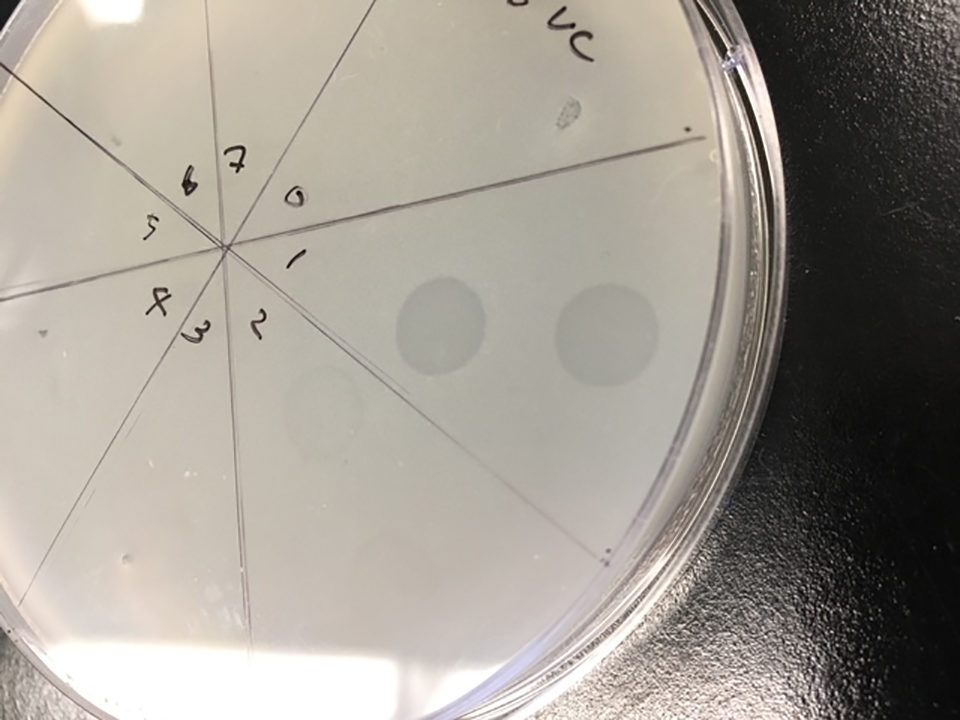
Perspectivas
En nuestro estudio, demostramos que los fagos aislados evaluados son efectivos para controlar la infección por AHPND e inhibir el crecimiento bacteriano cuando se aplica al camarón. Se necesitan más estudios para evaluar la eficacia de los bacteriófagos contra AHPND en ensayos de laboratorio y de campo.
Authors
-

Jee Eun Han, DVM, Ph.D.
Biotechnology Research Institute
CJ CheilJedang, Korea[32,109,111,99,46,108,105,97,109,103,64,51,50,50,49,101,106,110,97,104]
-

Kathy F.J. Tang, Ph.D.
Yellow Sea Fisheries Research Institute
Chinese Academy of Fishery Sciences, China[32,109,111,99,46,108,105,97,109,103,64,110,111,115,108,101,110,103,110,97,116,107]
-

Angela Corbin, M.S.
Assistant Professor
Department of Biological Science
Nicholls State University, USA[32,117,100,101,46,115,108,108,111,104,99,105,110,64,110,105,98,114,111,99,46,97,108,101,103,110,97]
Tagged With
Related Posts

Health & Welfare
Cuatro cepas de AHPND identificadas en granjas de camarón de América Latina
Se conocen dos genes de virulencia que codifican una toxina binaria de Photorhabdus relacionada con insectos que causa la enfermedad de necrosis hepatopancreática aguda en camarones. Las patogenicidades de estas cepas de V. campbellii fueron evaluadas mediante infección de laboratorio y posterior examen histológico en camarones P. vannamei.

Health & Welfare
EHP es un factor de riesgo para otras enfermedades del camarón
Desafíos de laboratorio y un estudio caso-control se utilizaron para determinar los efectos de la infección por EHP en dos enfermedades de Vibrio: necrosis hepatopancreática aguda (AHPND) y necrosis hepatopancreática séptica (SHPN).

Health & Welfare
Herramienta diagnóstica no-invasiva desarrollada para la enfermedad EMS del camarón
La presencia de AHPND-Vibrio parahaemolyticus puede ser detectada tanto en muestras de ADN fecal como en caldo bacteriano enriquecido con muestras de caldo de enriquecimiento que muestran mayor sensibilidad.

Health & Welfare
Acuamimetismo: Un concepto revolucionario para el cultivo de camarón
El acuamimetismo simula las condiciones de producción naturales estuarinas mediante la creación de floraciones de zooplancton como nutrición suplementaria para los camarones cultivados, y bacterias beneficiosas para mantener la calidad del agua. Se pueden producir camarones de mejor calidad a un costo menor y de manera más sostenible.

